ค่า Ph กรด – Ph ของเลือด: ระดับปกติการเปลี่ยนแปลงอาการการทดสอบและอื่น ๆ - ทางการแพทย์ - 2022
- The Face Shop โคราช
- แปลน-โรง-พยาบาล
- ค่าความเป็นกรด-ด่างของปัสสาวะ (urine pH หรือ pH) คืออะไร ?
- สถาบันวิจัยและพัฒนาพลังงานนครพิงค์ มหาวิทยาลัยเชียงใหม่
- ค่า pH - ค่าความเป็นกรด-เบส (pH), การทำให้เจือจาง, ความเข้มข้น - PhET
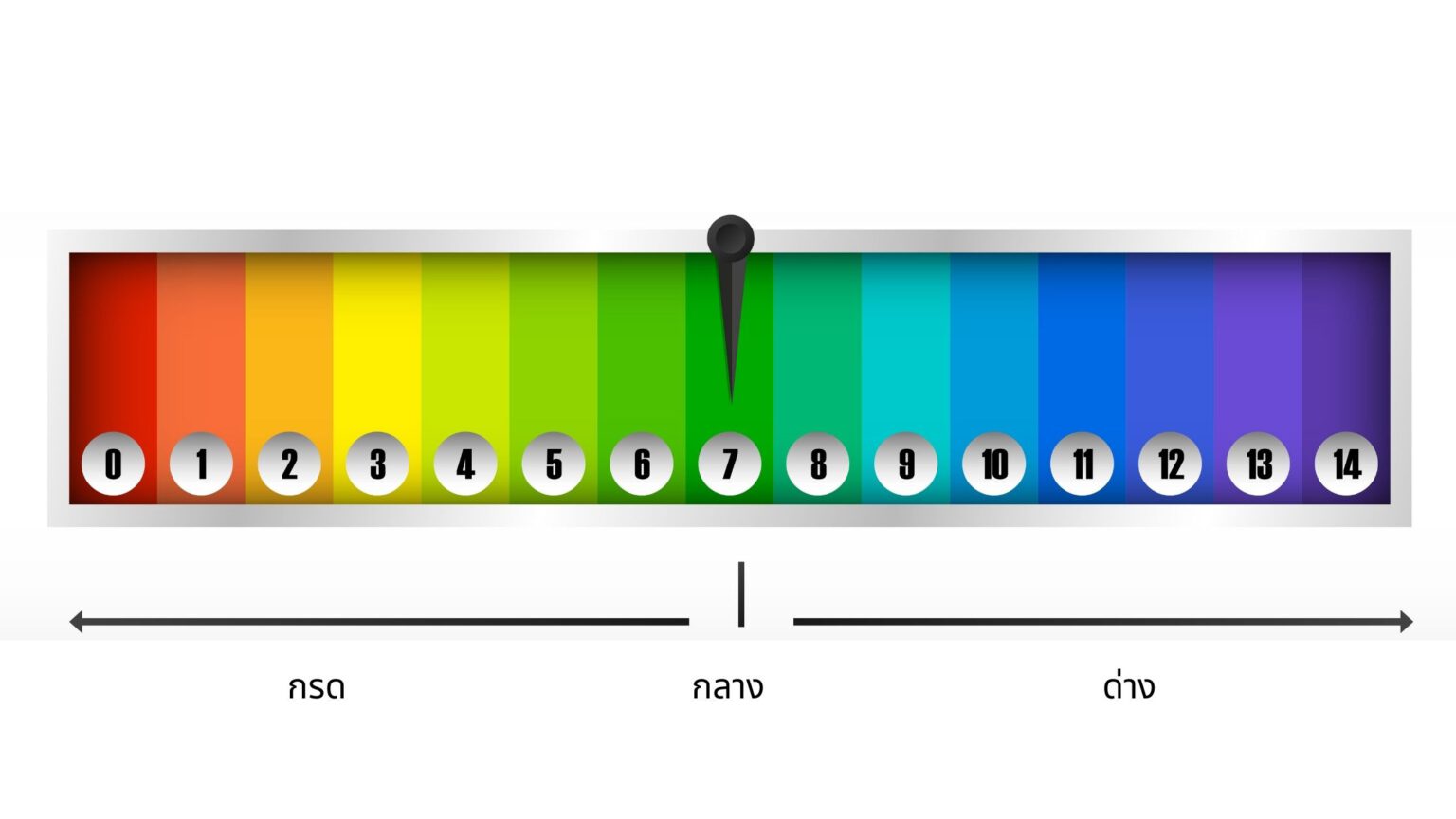
JILGYUNGYI ARTICLE บทความดีๆ ที่ช่วยเสริมความมั่นใจให้สาวจิลยอง 7 ตุลาคม 2562 ค่า pH คืออะไร? pH คือ ค่าความเป็นกรด (Acidic) หรือด่าง (Alkaline) ของสารต่าง ๆ หรือในสภาวะแวดล้อมแต่ละแห่ง โดยมีค่าเป็นตัวเลข ตั้งแต่ 0 ถึง 14 ซึ่งค่าที่ต่ำกว่า 7 ลงมา จะถือว่ามีสภาพเป็นกรด และค่าที่มากกว่า 7 ขึ้นไป จะถือว่ามีสภาพเป็นด่าง ส่วนค่า pH 7 นั้นจะมีสภาพเป็นกลาง ยกตัวอย่าง เช่น น้ำบริสุทธิ์ เป็นต้น ค่า pH มีความสัมพันธ์กับสมดุลช่องคลอดอย่างไร? ค่า pH มีบทบาทสำคัญต่อสภาพแวดล้อมที่อยู่ภายในช่องคลอด (Vagina) และสามารถบ่งบอกได้ว่าช่องคลอดของคุณมีสุขภาพที่ดีหรือไม่ ค่า pH ที่ทำให้ช่องคลอดเกิดความสมดุล หรือ pH Balance ของช่องคลอด ควรมีค่าเท่าไหร่? โดยกติแล้ว ค่า pH ของช่องคลอด หรือ pH Balance จะอยู่ระหว่าง 3. 8-4. 5 หรือ มีสภาพเป็นกรดอ่อน ๆ ซึ่งอาจแตกต่างกันเล็กน้อยในแต่ละบุคคล และเกิดการเปลี่ยนแปลงเมื่อเปลี่ยนช่วงวัยในชีวิต หรือมีการเปลี่ยนแปลงของฮอร์โมน ยกตัวอย่างเช่น เมื่ออยู่ในช่วงวัยเจริญพันธุ์ (Reproductive) อายุประมาณ 15-49 ปี ค่า pH ที่เหมาะสม และทำให้เกิดความสมดุลของช่องคลอด คือ pH ต่ำกว่าหรือเท่ากับ 4.
ค่าความเป็นกรด-ด่างของปัสสาวะ (urine pH หรือ pH) คืออะไร ?


วิธีเปรียบเทียบสี วิธีนี้เป็นการวัด pH โดยประมาณ (มีความถูกต้อง 0. 5 หน่วย pH) ซึ่งทำได้โดยเติมอินดิเคเตอร์ที่เหมาะสมลงไปในสารละลายที่ต้องการวัด pH แล้วเปรียบเทียบกับสารละลาย ทำได้โดยเติมอินดิเคเตอร์ที่เหมาะสมลงไปในสารละลายที่ต้องการวัด pH แล้วเปรียบเทียบสีกับสารละลายบัฟเฟอร์ที่ทราบค่า pH แน่นอน ซึ่งได้เติมอินดิเคเตอร์ชนิดเดียวกันไปแล้ว หรือใช้กระดาษชุบอินดิเคเตอร์ (กระดาษ pH) จุ่มลงไปแล้วเปรียบเทียบกับสีมาตรฐาน 2. วิธีวัดความต่างศักย์ วิธีนี้วัด pH ได้อย่างละเอียด (มีความถูกต้อง 0. 01 หน่วย pH) โดยการใช้ pH Meter ซึ่งวัด pH ของสารละลายได้โดยการวัดความต่างศักย์ระหว่างขั้วไฟฟ้า 2 ขั้ว ภาพ pH Meter VDO การใช้ pH Meter
00 นอกจากนี้สามารถบอกความเป็นกรด-เบสของสารละลายในรูปความเข้มข้นของ OH – ก็ได้ โดยค่า pOHค่า pOH ใช้บอกความความเป็นกรด- เบสของสารละลายเจือจางได้เช่นเดียวกับค่า pH ซึ่งค่า pOH จะขึ้นอยู่กับความเข้มข้นของ OH – โดยกำหนดความสัมพันธ์ดังนี้ ตัวอย่างการคำนวณค่า pOH สารละลาย NaOH เข้มข้น 0. 01 โมลต่อลูกบาศก์เซนติเมตร มี pH เท่าใด วิธีทำ NaOH (aq) ————-> Na + (aq) + OH – (aq) 0. 01 mol/dm 3 0. 01 mol/dm 3 = 1 x 10 -2 mol/dm 3 pOH = -log[OH –] = -log 1×10 -2 mol/dm 3 = 2log10 – log1 pOH = 2 ในสารละลายที่เป็นกลางซึ่งมี [OH –] = 1. 0 x 10 -7 mol/dm 3 จะมี pOH = 7 ความสัมพันธ์ระหว่าง pH กับ pOH [H 3 O +][ OH –] = 1. 0 x 10 -14 log[H 3 O +][ OH –] = log1. 0 x 10 -14 log[H 3 O +] + log[OH –] = log1. 0 – 14 log10 – log[H 3 O +] – log[OH –] = 14 log10 มาตราส่วน pH (pH scale) ใช้บอกความเป็นกรด-เบสของสารละลาย ตารางแสดง สเกล pH ของสารละลายที่มีความเข้มข้นต่างๆ กัน วิธีวัด pH ของสารละลายวัดได้ 2 วิธี ดังนี้ 1. วิธีเปรียบเทียบสี วิธีนี้เป็นการวัด pH โดยประมาณ (มีความถูกต้อง 0. 5 หน่วย pH) ซึ่งทำได้โดยเติมอินดิเคเตอร์ที่เหมาะสมลงไปในสารละลายที่ต้องการวัด pH แล้วเปรียบเทียบกับสารละลาย ทำได้โดยเติมอินดิเคเตอร์ที่เหมาะสมลงไปในสารละลายที่ต้องการวัด pH แล้วเปรียบเทียบสีกับสารละลายบัฟเฟอร์ที่ทราบค่า pH แน่นอน ซึ่งได้เติมอินดิเคเตอร์ชนิดเดียวกันไปแล้ว หรือใช้กระดาษชุบอินดิเคเตอร์ (กระดาษ pH) จุ่มลงไปแล้วเปรียบเทียบกับสีมาตรฐาน 2.
สถาบันวิจัยและพัฒนาพลังงานนครพิงค์ มหาวิทยาลัยเชียงใหม่
ศ. 2555 ดังนี้ 1. ค่า pH ว่าน้ำแต่ละยี่ห้อมีความเป็นกรด-ด่างมากน้อยเพียงใด ค่า pH ต่ำกว่า 7 เป็นกรด และยิ่งเป็นกรดมากเมื่อมีค่า pH ต่ำ เป็นด่างเมื่อค่า pH สูงกว่า 7 และยิ่งเป็นด่างมากมื่อค่า ph สูงขึ้น 2.
- ปุ่มรองเท้ากอล์ฟ footjoy
- PH ของสารละลาย - กรด-เบส
- เปรียบเทียบผลสำรวจ "กรด-ด่าง" น้ำดื่มและน้ำอัดลม 21 ยี่ห้อ
- ค่า pH คืออะไร ระดับความเป็นกรด-ด่าง ที่ดีต่อผิวพรรณของเรา - PSA SUPPLY
- ทิศ กับ ธาตุ s
- The pizza company ระยอง
- 2022 Serbia League Women,ผลบอลและตารางคะแนนบอล ----- thscore
- All star tower defense โค้ด
- Nova 2i แบ ต 2
- เข้าใจค่า pH ดินและวิธีการตรวจวัด
- RICOH XR500 AUTO - ฟิล์มคาเมร่า เชียงใหม่ซ๊อป : Inspired by LnwShop.com
75 ค่า ORPอยู่ที่ +353 มิลลิโวลต์ 5. น้ำอัดลม อาเจบิ๊ก ส้ม ค่า pH อยู่ที่ 2. 61 ค่า ORP อยู่ที่ +351 มิลลิโวลต์ 6. น้ำอัดลม โคคาโคล่า ซีโร่ ค่า pH อยู่ที่ 2. 56 ค่า ORP อยู่ที่ +340 มิลลิโวลต์ 7. น้ำอัดลม โคคาโคล่า ไลท์ ค่า pH อยู่ที่ 2. 55 ค่า ORP อยู่ที่ +333 มิลลิโวลต์ 8. น้ำอัดลม เป๊บซี่ แมกซ์ ค่า pH อยู่ที่ 2. 46 ค่า ORP อยู่ที่ +333 มิลลิโวลต์ 9. น้ำอัดลม อาเจบิ๊ก โคล่า ค่า pH อยู่ที่ 2. 23 ค่า ORP อยู่ที่ +379 มิลลิโวลต์ 10. น้ำอัดลม โคคาโคล่า ค่า pH อยู่ที่ 2. 13 ค่า ORP อยู่ที่ +342 มิลลิโวลต์ 11. น้ำอัดลม เป๊บซี่ ค่า pH อยู่ที่ 2.
ค่า pH - ค่าความเป็นกรด-เบส (pH), การทำให้เจือจาง, ความเข้มข้น - PhET
5 กันดีกว่าค่ะ ซึ่งวิธีที่ง่ายที่สุดคือการอาบน้ำด้วยสบู่ที่มีกรดอ่อน ๆ และบำรุงผิวด้วยครีมบำรุงผิวที่มีส่วนผสมของสารสกัดจากธรรมชาติเป็นประจำทุกวัน เพราะนอกจากจะช่วยปรับสภาพผิวให้คงทีแล้วยังช่วยฟื้นฟูบำรุงผิวกายที่แห้งเสียได้อย่างมีประสิทธิภาพด้วยค่ะ
ผู้ช่วยศาสตราจารย์ ดร. นิวัฒน์ ศรีสวัสดิ์ กลุ่มวิจัยการศึกษาวิทยาศาสตร์และเทคโนโลยีแนวใหม่ สาขาวิชาวิทยาศาสตร์ศึกษา คณะศึกษาศาสตร์ มหาวิทยาลัยขอนแก่น (สนับสนุนโดยสำนักงานเลขานุการกองทุนพัฒนาเทคโนโลยีเพื่อการศึกษา กระทรวงศึกษาธิการ)
ในสารละลายกรดหรือเบสจะมีทั้ง H 3 O + และ OH – อยู่ในปริมาณที่แตกต่างกัน การบอกความเป็นกรด เป็นเบสของสารละลายโดยใช้ความ เข้มข้นของ H 3 O + หรือ OH – มักเกิดความผิดพลาดได้ง่ายเพราะสารละลายมักมีความเข้มข้นของ H 3 O + หรือ OH – น้อย ดังนั้นในปี ค. ศ. 1909 นักเคมีชาวสวีเดนชื่อ ซอเรสซัน (Sorensen) ได้เสนอให้บอกความเป็นกรด-เบสของสารละลายในรูปมาตราส่วน pH ย่อมาจากภาษาฝรั่งเศสว่า puissance d, hydrogine แปลว่า กำลังของไฮโดรเจน (power of hydrogen) โดยกำหนดว่า เมื่อความเข้มข้นของ H 3 O + มีหน่วยเป็น mol/dm 3 หรือ Molar ในสารละลายที่เป็นกลาง [H 3 O +] = [OH –] = 1. 0 x 10 -7 mol/dm 3 ดังนั้น หา pH ของสารละลายได้ดังนี้ pH = – log[H 3 O +] = – log 1. 0 x 10 -7 = – (log 1. 0 – 7log10) = 0 + 7 = 7 นั่นคือสารละลายที่เป็นกลางมี pH = 7 ค่า pH ที่ใช้ระบุความเป็นกรดหรือเบสของสารละลาย สรุปได้ดังนี้ สารละลายกรด มี [H 3 O +] มากกว่า 1. 0 x 10 -7 mol/dm 3 ดังนั้น pH<7. 00 สารละลายที่เป็นกลาง มี [H 3 O +] เท่ากับ 1. 0 x 10 -7 mol/dm 3 ดังนั้น pH = 7. 00 สารละลายเบส มี [H 3 O +] น้อยกว่า 1. 0 x 10 -7 mol/dm 3 ดังนั้น pH>7.